37.5 愈合与营养
若术前营养状况良好,术后进入至创伤反应第二阶段时,尽管机体尚处于负氮平衡时期,伤口或切口若无感染,则可迅速开始愈合,表现伤口占有“优惠地位”,以身体其他部位的组织和肌肉为营养素的提供者,用来合成胶原以使伤口愈合。在创伤后第三阶段,若外源营养素供给充裕,则一方面伤口仍处于“优惠地位”,不断摄取营养素;另一方面,身体其它组织和器官可减少消耗,并且也获得营养补充,则能转为正氮平衡,身体逐日康复。
若术前营养不良,术后又未注意营养支持,则即使伤口处于“优惠地位”,因缺少物质基础也难以愈合。营养不良时,机体的免疫功能受损,易继发感染。若感染未很好控制,营养又未很好补充,持续过久,则伤口愈合缓慢,甚至停顿。如临床所见的延迟不愈的肠瘘,烧伤病人屡次植皮失败以及骨折病人骨不连合等。
对于未感染的手术切口,术后7天左右,愈合的切口,其抗张强度已达到病人可从事一般的活动。污染的较大伤口,经清创暴露后,一般于伤后第5~15天为二期愈合*的良好时机,在Ⅲ°烧伤,伤后第12~21天为植皮良好时机,超过30天以上,则植皮的成活率受影响。若能得到及时的营养支持,则能改善其情况。
下面将讨论伤口愈合与骨折愈合与营养的关系。
37.5.1 伤口愈合与营养
(1)伤口愈合的组织形态学变化
①炎症:组织损伤后,损伤处即出现炎症反应。毛细血管扩张、渗透性增加、淋巴管为纤维蛋白所阻塞、出现轻微红肿的现象。对合伤面间隙中的血液、淋巴液及组织渗出液凝结成血块,使两侧伤面粘合,并使伤面渗血停止。渗出的白细胞等将细胞破片和碎屑除去。清洁的切口,急性炎症一般在几天内即消失。
②上皮形成:于伤后24h内,紧靠伤口边缘的上皮开始增厚。边缘的基底细胞失去对下面真皮的坚固附着,经迅速的有丝分裂,向下增殖,并跨过缺隙处。在48h内,整个伤口表面重新上皮化。
③细胞期:当炎症反应消退和上皮的表面增厚时,伤口深部出现成纤维细胞,从伤后第2天或第3天开始到第10天,即在细胞总数中占优势。成纤维细胞合成并分泌胶原分子。在电子显微镜下,成纤维细胞的外观是典型的。除了弥散的高尔基体和粗大不规则嵴的线粒体之外,含有一个明显发育和扩张的粗面内质网。长而互通的池,由弯曲的双排多体畸形形成边界,附着在浆膜上。
除成纤维细胞外,在缝合24h后,伤面组织内的毛细血管内皮细胞向凝块内生长,形成新的毛细血管网,供应新生组织所需营养并排出代谢产物。
④纤维组织形成:到第4或第5周,成纤维细胞的绝对数量明显减少,并且也不再具有活跃的内质网,而胶原纤维却成了占优势的结构表现。最初的胶原纤维出现在第4~5天。伤口间隙很快充满了小而杂乱定向的纤维束。纤维束逐渐增大,并形成大量致密的胶原组织(瘢痕),将切断的组织牢固地缚地一起。丰富的毛细血管网缩小为少数成形的毛细血管系统,贯穿瘢痕终生。
以上变化可简括为:对合的切面首先出现炎症,间隙被渗出物所填充,继之成纤维细胞增多,生成胶原纤维组成结缔组织,将两侧连接起来,同时上皮覆盖,完成愈合。
(2)伤口愈合的生化变化与营养的关系
①炎症:20世纪初期以来,一系列研究说明,由损伤部位的肥大细胞、颗粒细胞和血小板释放的组织胺,能引起局部血管扩张和增加小血管通透性,是炎症反应的主要介质。近来,更认识到组织损伤时释放出的激肽和前列腺素(主要是前列腺素E1和E2)在导致急性炎症中起决定性作用。
已知人和哺乳动物体内含有三种激肽,即缓激肽、胰激肽和蛋氨酰胰激肽。这三种激肽分子内部都含有缓激肽的9肽结构(H.精—脯—脯—甘—苯丙—丝—脯—苯丙—精.OH),因而有相类的作用,其中缓激肽的活性最强。当组织损伤时,由于血管内皮暴露出胶原或组织蛋白酶的释放,可引起一系列的酶促反应,使血浆或组织中的激肽原(由肝脏以氨基酸及糖类为原料合成而来)转变为缓激肽。
前列腺素最初在前列腺中发现,后来知道,几乎身体内一切组织都可以不饱和脂肪酸为原料在激肽系统影响下转变为前裂腺素。前列腺素E1及E2即分别由花生三烯酸及花生四烯酸转变而来。
②结缔组织:从组织学看,结缔组织是由包埋于无定形而内含组织液的基质中的细胞和细胞外的纤维所组成。即结缔组织主要由细胞、基质及纤维所组成。基质是无定形的胶状物质,其化学成分主要是蛋白多糖(即粘蛋白)。纤维包括胶元纤维、网状纤维及弹性纤维。在伤口愈合中以胶元纤维为主。现分别讨论蛋白多糖及胶原纤维:A.蛋白多糖,其分子结构是一条肽链上联结许多条氨基多糖链,象瓶刷的形状。故分子中蛋白质比例小而多糖链的比例大。结缔组织中常见的氨基多糖有以下数种(表37-2)。
从表中可见,除透明质酸不含硫酸外,其他皆含硫。已知氨基多糖是在成纤维细胞的粗面内质网,当新合成的多肽链在内质网移行时,各种单糖及其衍生物(N-乙酰氨基已糖及葡萄糖醛酸),受相应的糖基转移酶的催化,按一定的顺序连接到肽链的一定部位而合成氨基多糖。硫酸的掺入是在硫酸转移酶的催化下,将活性硫酸(3′—硫酸腺苷—5′—磷酸硫酸)中的硫酸转移到新合成的氨基多糖链上去。实验证明维生素A缺乏时,硫酸转移酶的活性下降,故缺乏维生素A时,氨基多糖合成受阻,这可能是维生素A缺乏时,伤口愈合迟缓,以及生长期的动物,组织生长及发育障碍的原因;B.胶原纤维,其化学成分是胶原蛋白,简称胶原,是由成纤维细胞合成。它是由许多原胶原分子整齐地定向排列,并通过共价键交联所形成的稳定而不易溶解的胶原分子。它在电子显微镜下呈现原纤维的形态。原纤维平行聚集成束就是胶原纤维。每个原胶原分子都由三条α-肽链以三股螺旋状结构所组成。
原胶原分子中的α-肽链,在组成和结构中有如下两个特点:A.在氨基酸排列顺序中,每隔两个其他氨基酸(以x及y代表)即有一个甘氨酸,故肽链结构基本上可用(甘-x-y)n来表示。从这一公式中可看出甘氨酸在胶原分子中所占的比重;B.组成的氨基酸中含有约11~12%的羟脯氨酸和羟赖氨酸,以及脯氨酸和羟脯氨酸合在一起约占21~22%,甘氨酸、脯氨酸、羟脯氨酸三者总和约占50~53%,这在其他蛋白质中是很少见的。这从表37-3中即可看出这两个特点。
表37-2 结缔组织中常见的氨基多糖
| 名称 | 基本结构单位 |
| 透明质酸 | 葡萄糖醛酸,N-乙酰氨基葡萄糖 |
| 硫酸软骨素A | 葡萄糖醛酸,4-硫酸-N-乙酰氨基半乳糖 |
| 硫酸软骨素C | 葡萄糖醛酸,6-硫酸-N-乙酰氨基半乳糖 |
| 硫酸软骨素B | 艾杜糖醛酸,4-硫酸-N-乙酰氨基半乳糖 |
| 硫酸角质素 | 半乳糖,6-硫酸-N-乙酰氨基葡萄糖 |
注:肝素也属于氨基多糖,主要存在于肺、皮肤、肝、肠等肥大及啫碱性白细胞内。
从表37-2可见,在氨基酸品种方面 除羟赖氨酸和羟脯氨酸外,胶原所含有的氨基酸,肌球蛋白及肌动蛋白都含有,而羟赖氨酸和羟脯氨酸在胶原合成中,可以赖氨酸和脯氨酸为原料。赖氨酸为必需氨基酸,而脯氨酸为非必需氨基酸,很容易从谷氨酸转变而来。所以,以肌球蛋白及肌动蛋白作为氨基酸的提供者以合成胶原时,在氨基酸品种上是可以满足的。只是在各种氨基酸的比例上,由于胶原较肌球蛋白及肌动蛋白富含甘氨酸、脯氨酸、丙氨酸和羟脯氨酸。因此,将消耗远远多于所合成胶原的量,才能提供所需的各种氨基酸。在进食量不足,依靠内源性肌肉蛋白来完成伤口愈合是不经济的。故术后应尽可能早地使病人得到外源蛋白质,并且考虑到氨基酸品种上的特点,适当给以富含甘氨酸、脯氨酸、丙氨酸和羟脯氨酸的食物,或直接给以富含胶原的猪皮或猪蹄之类作成的食物,如猪皮冻或猪蹄汤(包括汤和猪蹄皮),是有极大益处的。
表37-3 肌球蛋白、肌动蛋白及胶原的氨基酸含量比较表(mol·105g-1)
| 氨基酸种类 | 肌球蛋白 | 肌动蛋白 | 胶原 |
| 赖氨酸 | 94 | 47 | 31 |
| 组氨酸 | 17 | 18 | 5 |
| 精氨酸 | 46 | 38 | 49 |
| 门冬氨酸 | 82 | 86 | 47 |
| 苏氨酸 | 36 | 62 | 19 |
| 丝氨酸 | 45 | 53 | 32 |
| 谷氨酰胺 | 166 | 99 | 77 |
| 脯氨酸 | 20 | 46 | 131 |
| 甘氨酸 | 41 | 70 | 363 |
| 丙氨酸 | 75 | 72 | 107 |
| 胱氨酸 | 8 | 12 | - |
| 缬氨酸 | 42 | 48 | 29 |
| 蛋氨酸 | 24 | 38 | 5 |
| 异亮氨酸 | 42 | 64 | 43 |
| 亮氨酸 | 86 | 65 | 43 |
| 酪氨酸 | 17 | 38 | 5 |
| 苯丙氨酸 | 30 | 30 | 15 |
| 羟赖氨酸 | - | - | 7 |
| 羟脯氨酸 | - | - | 107 |
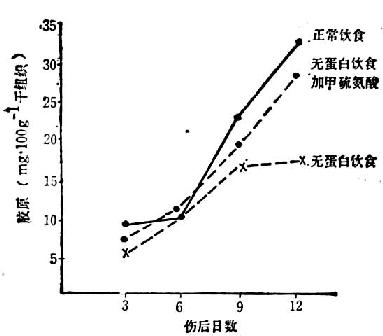
胶原的合成与含硫氨基酸的关系:实验研究以及临床上早已观察到蛋白质缺乏影响伤口愈合,通过补给含硫氨基酸(甲硫氨酸或酰氨酸)可获得改善(图37-3)。最近证明在胶原的合成过程中,最初在细胞内合成的肽链,比可以聚集为胶原分子的肽链要长得多,约长30~40%(原胶原)。其坚硬中心的两端非螺旋形的肽含有半胱氨酸。非螺旋形端的迅速联合以及双硫键的形成,促进定位和坚硬中心的螺旋形集合,然后在前胶原肽酶的作用下,含半胱氨酸的非螺旋形部位从分子上脱落下来,中心成螺旋交联部分即为胶原。故胶原分子中不含半胱氨酸,但却是合成过程所必需。
胶原的合成与Cu2+的关系:三和要肽链组成的原胶原分子,在最初阶段,其张力强度是较弱的。随着时间的推移,在三条肽链之间或邻近分子之间形成共价键,张力强度才得以增加。虽然胶原纤维中的分子内和分子间的共价键的性质还在研究之中,但某些键反应已被确定。如二条肽链之间赖氨酸的交叉连接。赖氨酸先转变为醛,二条肽链上的醛基藉醛醇缩合反应而连接起来。

图37-3 伤口愈合与蛋白质的关系
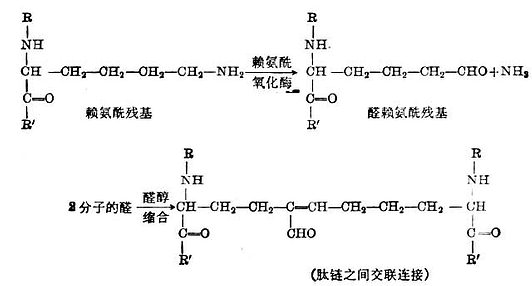
在赖氨酰氧化酶催化赖氨酸变成δ-半醛-α-胺已二酸的反应中需要铜离子为辅助因子。铜的耗竭或不足将影响醛醇缩合及交联连接。
胶原的合成与Fe2+和抗环血酸的关系:胶原合成中还有一个特点,即脯氨酸或赖氨酸不是先羟基化为羟脯氨酸或脯氨酸或羟赖氨酸之后再合成胶原,而是脯氨酸或赖氨酸参与合成原胶原以后,再由脯氨酰羟化酶使肽链上的脯氨酸羟基化。羟基化过程中,羟基中的氧原子来自空气中的分子氧,以及脯氨酰羟化酶需要-α酮戊二酸作为基质和二价铁为辅助因子,还需要抗坏血酸作为电子供体。故铁和抗坏血酸是伤口愈合所必需。一般未感染的切口,术后7天左右,其胶原形成,已使病人从事一般的活动而不至裂开。此时可拆线出院,但伤口胶原的形成和交联可持续数月或经年,这时期仍需不断补充抗坏血酸,若缺乏出现坏血症,切口在外力作用下,尚有裂开的可能。
伤口愈合与锌的关系:由于锌是体内许多种酶的成分或辅酶的成分,特别锌是DNA聚合酶、RNA聚合酶的辅酶成分,对细胞的分裂生长以及蛋白质的合成都有密切的关系。与伤口愈合密切相关的蛋白多糖和胶原纤维,在化学成分上都属于蛋白质。故锌也影响它们的合成。不仅如此,锌对伤口年上皮的形成,影响更为显著。这从锌影响细胞分裂、生长及蛋白质合成以及体内20%的锌存在于皮肤中,尤其集中在上皮组织可得到解释。经许多学者研究肯定,机体处于低锌状态时,补锌是有促进作用的。而应激时(如手术)随尿氮、尿磷、尿硫等排出增加,尿锌排出也是增加的。术后恢复期,机体无疑处于低锌状态。临床上有的以硫酸锌或醋酸锌补充外,食物中,动物皮肤含量都很高,当以猪皮或猪蹄作为获得甘氨酸、脯氨酸的来源时,同时也获得了较多量的锌。
综上所述,可见伤口愈合与含硫氨基酸、甘氨酸、脯氨酸(羟脯氨酸)、赖氨酸(羟赖氨酸)、维生素A、抗坏血酸以及铁、铜、锌的密切关系。而蛋白质丰富、热量充裕的完全而平衡的营养对术后机体恢复和保证伤口愈合的重要性是无需赘述的。
37.5.2 骨折修复与营养
先从骨的结构和组成,再结合骨折修复及影响因素来讨论应注意的营养问题。
(1)骨的结构和组成
①骨的大体结构:用肉眼或一般的放大镜观察,可把骨分为两种类型——松质骨和密质骨。松质骨由分枝的骨小梁的主体网格构成,形成一个间隙互相连通的错综复杂的系统,内面充满骨髓。密质骨呈实心的连续体,在显微镜下才能看到其中的间隙。
②骨的微细结构:如用显微镜观察长骨骨干薄磨片,可观察到密质骨主要由钙化了的骨基质所组成,称为骨板。在骨基质中均匀地遍布着腔隙,称为骨陷窝。每一个骨陷窝中有一个骨细胞。从每个骨陷窝向四周辐射状伸出骨小管,与邻近骨陷窝的骨小管相吻合,形成广泛的纤细通道。并与最近的血管周围间隙相通以获取营养、交换离子、维持骨的正常代谢。上述密质骨的骨板常围绕骨内的纵行血管通道呈同心圆排列,形成圆柱形结构单位,称为哈弗系统。松质骨也由骨板组成,但骨小梁较细,一般没有血管进入,故没有哈弗系统。骨细胞的营养从骨内膜表面,经微细的骨小管弥散而来。
从以上所述,可知骨主要由细胞和骨基质两部分组成。
①骨的细胞:包括骨细胞、成骨细胞、破骨细胞及其他细胞等。是由间充质细胞根据骨化的不同情况,所分化出不同形态和不同功能的细胞。成骨细胞是合成骨基质中的胶原和蛋白多糖的细胞。在合成作用旺盛时呈方形,细胞内可见合成蛋白质以供分泌的超微结构——发达的粗面内质网和高尔基体。胶原和蛋白多糖由粗面内质网合成后,由细胞表面排出到细胞外,无机物借胶原而沉积。当成骨细胞一旦被新合成的基质完全包围,它就在骨陷窝中成为骨细胞。破骨细胞仅出现在骨质吸收和骨分解时骨的表面,能分泌胶原蛋白酶、蛋白水解酶等使胶原纤维分解,骨基质解聚。骨折后骨折部位也出现破骨细胞,以清除被损骨质的残屑和钙盐。其他细胞有网状细胞、骨内膜细胞(实质上是静止的成骨细胞)以及成纤维细胞(当它增值时,将合成胶原)。
②骨基质:又可分为有机物和无机物两部位。其中有机物大部分为胶原,称为骨胶原,骨胶原的结构和普通结缔组织的胶原基本一样,也是以等距离横纹的纤维形式出现,由转化来的成骨细胞的粗面内质网所分泌而进入细胞间隙的。在成熟的板层状骨内,胶原纤维的排列非常规整。在哈费系统的每一块骨板内,胶原纤维平行排列,有机物中除胶原外则为无定形基质,包括硫酸软骨素A、硫酸软骨素C、硫酸软骨素B、硫酸角质素以及透明质酸,也由成骨细胞所分泌。至于无机物则占骨基质干重的50~65%,主要成分是磷酸钙(占84%),其他碳酸钙占10%,柠檬酸钙占2%,磷酸镁占1%,磷酸氢二钠占2%。无机物中有60%以结晶的羟磷灰石[Ca10(PO4)6(OH)2]的形式存在。其余40%为无定形的磷酸氢钙,Ca2+、Mg2+、Na+、Cl-、HCO3-、F-以及柠檬酸根可吸附在羟磷灰石微细结晶的晶格之间。电镜下见羟磷灰石晶体呈长条状结晶,位于胶原原纤维侧畔,并经常被一层无定形基质所包裹。羟磷灰石的表面离子是同水结合的,形成一个水化层,利于晶体和体液进行离子交换。
以上是正常情况,骨折时新骨的形成及修复的过程如下:
(2)骨折修复
①骨痂形成的组织学变化:骨折后血肿充满组织间的裂隙。断端附近的骨细胞因受伤和缺血而坏死。邻近断端的骨外膜于骨折后24h即出现组织学变化。深层的细胞增加,胞核增大。一周后在增厚的骨外膜中,出现于骨干平行并紧密相连的片状骨样组织。
②此时,由于血肿尚未机化,新生的细胞血管尚未深入,故骨外膜处的成骨细胞的分泌和活动只能沿着血肿外圈向骨折处推进。随着血肿的机化,骨折处骨内膜也出现组织学变化,逐渐骨折两端由骨外膜生成的外骨痂和由骨内膜生成的内骨痂分别会合。最终血肿完全机化,内外骨痂会合成桥梁骨痂。当完全融合并完全骨化时则达到临床愈合。以后经过塑形期,骨痂密度加大,骨折间隙完全消失,则达到骨性愈合。
(3)骨折修复的生化变化与营养的关系
①成骨细胞分泌无定形基质蛋白多糖以及胶原,其生化变化与切口愈合中成纤维细胞的生化过程相同。
②在胶原上沉积无机物使成为骨样组织。由于钙在无机物中占的比例最大,故这一过程称为骨的钙化。要使体液中离中状态的无机盐转为固体沉积下来,首先在钙化的局部要有足量的钙和磷酸根离子,这就涉及到膳食中的摄入量是否丰富以及维生素D是否充裕,或接受紫外光线或日光是否充足。然后由于碱性磷酸酶的作用(在腺三磷的协同下),使胶原钙化。钙化最先在交错排列的胶原原纤维末端之间的空隙处开始,先沉积的钙盐结晶很小,随着不断地沉积慢慢加大,填充在基质内。
碱性磷酸酶能水解多种磷酸酯,使无机磷离子浓度升高,并使钙化抑制剂焦磷酸盐水解,解除对钙化的抑制,故在钙化中的作用很重要。而碱性磷酸酶是含锌的酶,锌的充裕与否影响其活性。家兔骨折实验中,供锌组骨痂中锌含量明显高于对照组,并且骨折愈合加快,抗拉伸性能优于对照组。组织学检查观察到细胞增强活跃,软骨及新骨丰富,X线显示丰富的外骨痂。并观察到无论供锌组或对照组,凡骨折的家兔,其桡骨的非骨折部位以及尺骨中的钙和锌的含量均明显下降。在8周的观察期内,骨锌含量皆低于正常值。说明骨折后机体动员体内非骨折部位的骨钙、骨锌以保证骨折部位的愈合。这一实验结果充分说明,骨折后补充锌的重要性。锌的作用不仅仅在于是碱性磷磷酸酶的成分。还关系到胶原的合成。
由于骨折修复的第一步是胶原和蛋白多糖的合成,凡影响胶原和蛋白多糖合成的因素对骨折修复也有影响,如铜能促进骨折的愈合已为实验所证实。