�ڶ��ڡ�Ⱦɫ����
����һ�����Ʊ꿹�巨
����ø�꿹�弼����ͨ�����ۼ���ø�����ڿ����ϣ��Ƴ�ø�꿹�壬�ٽ�ø�Ե������������ã�������ɫ�IJ����Բ�������һ�������ܶȵĿ������ڹ⾵��羵�½���ϸ�����漰ϸ���ڸ��ֿ�ԭ�ɷֵĶ�λ��
������һ��ø�����༰�ص�
�����������Ͻ�����ϸ����ѧ��������ʾ��ø���������ڱ�ǿ��壬����ICCȾɫ����ʵ������ICC�������õ�ø�����ࡣ�ֽ����õļ���ø���ڱ�4-1����ѡ��ʱ�ο���
��4-1 ����ϸ����ѧ���õ�ø
| �� �� | �� �� �� | �� Դ �� | �� Ʒ |
| Horseeradish peroxidase(E.C.1,11,1,7) | 40��45KD | + | �� |
| Alkaline phosphatase (E.C.3,1,3,1) | 80��120Kd | ++ | �� |
| Acid phosphatase (E.C.3,1,3,2) | 100Kd | +++ | �� |
| Glucose oxidase | 160��190kD | �� | �� |
����Sternberger(1986)ָ�������ڱ�ǵ�øӦ�߱����¼����ø���ĵ������������ģ������ױ���ʾ�����γɵIJ������ڹ⾵��羵�¹۲죻�����γɵ��ղ�����������ȶ������ղ��ﲻ�ܴ�ø���Բ�λ����Χ��֯��ɢ��Ӱ����֯ѧ��λ���۽���õ�ø���ӣ��������Ʒ���ۣ�������pHʱ��øӦ�ȶ���ø��ǿ������1��2����Բ�Ӧ�ı䣬��ø�Ĵ����ԣ�Turnover��Խ��Խ�ã���ø������У�ø�뿹�����ᣬ����Ӱ����ߵĻ��ԣ��ޱ������֯�У���Ӧ��������ø��ͬ����Դ��ø���������ʡ�
�������У��٢�������Ϊ��Ҫ����Ϊ����������ʾ��ø�����γɲ������Եĸ����һ����Ϊ��������������ø��Horseradish peroxidase , HRP���ϼѣ�����õ�һ��ø��HRP�㷺�ֲ���ֲ��磬��ֲ������������ɽ�βˣ���Ҷ�ں�����ḻ����������������ɫ��ø��������ɫ����߲�������ɵ�һ���ǵ��ף���ռ16%��18��8�������ֲ���HRP���ӱ��棩��������40kD������pH5��5.5�������¶�40��45�棻 pH4��11��50�����¾����ȶ���������ˮ��58%���µı����������Һ��ø�Ļ������ĺ���߲�����Ƹ�����������չ���Ϊ403nm��������ǻ��Ե�ø���ײ������չ���Ϊ275nm��HRP�Ĵ������ö��ߵĹ��ܶȱ�ֵ��Od 403/275��������Reinheit Zahl (RZ)��ʾ��һ����Ϊ�����ø��RZֵΪ3.0���ң���ӦС��2.8��RZֵԽС��ø�Ĵ���Խ�����RZֵΪ0.6��ø�����ǻ��Ե�ø�������ߴ�75%�����ڴ��ȵ͡��������ø���贿����ʹ�á�
������HRP�⣬��������ø��Alkaline phasphotase, ALP��������������ø��Glucose oxidase, GOD��Ҳ�ϳ��á�ALP������ԼΪHRP��2��3��������pH9.0��9.5���ң��Ƚ��ȶ�����Դ��ALPҲ�����������־��ɱ���������Levamisole,������240.8kD�����ƣ�����ճĤ�������Դ��ALP���Բ���Ӱ�졣Ŀǰ���õ�ALP���ϵ��ţ�ij�ճĤ��ȡ�Ƶã����Գ�ճĤ�ȳ�ǿ���Է�Ӧ��
����ALP�������Bulman�����ڱ�ǿ���ġ�ѡ�ò�ͬ�ĵ�����γɲ�ͬ��ɫ���ղ�����������ӣ�As-Mx���Ϳ�����Fast Blue, FB��Ϊ���������ɫ�������ÿ�죨Fast Red, FR������FB���γɺ�ɫ���ܳ�������HRP/4-��-1-���ӣ�CN����DAB�γɵij����γ������Աȣ���FB��FR�ȳ����������л��ܼ������ܽ�����ˮ�����ȴ������ݱ��棬������Ʒ�죨New fuch��sine ����ɫ���γɵĺ�ɫ�������ﲻ�����л��ܼ�������ɫ����Ⱥ˸�Ⱦ���Ƴɰ������Ա���걾��
����GOD�����ĵ���Ϊ�����ǣ����ӹ���Ϊ��������������P-Nitroblue Tetrazolium��,�ղ���Ϊ�����Ե���ɫ�������Ƚ��ȶ����������Ͻ�GOD��ALP��HRPΪ�ѣ���Ϊ���鶯����֯�ڲ�������Դ��GOD������������ϴ��н϶�İ������ڱ��ʱ���γɹ㷺�ľۺϣ�Ӱ��ø�Ļ��ԣ���GOD��Ҫ����ICC˫��Ⱦɫ������ø�ķŴ�����
�������������Ʊ꿹����Ʊ���Boosma,DM, 1983��
����ø�꿹����ӫ��ɫ�ر�ǿ��岻ͬ�����������-ż���������ã���ø�����ڿ�������ϡ�ż������һ��˫�����Լ����߱�3��������������ż�����뿹���ø֮������ᣬ�����Dz�����ģ����蹲�ۼ������ż������ӦӰ��ø�Ϳ���Ļ��ԣ��۲�����ż�����ļ��룬ʹø����֯�ɷ������������ϡ�
������HRP��ǿ����У����õ�ż���������ȩ���������Ƽ�Maleimide�ȣ��ּ�����¡�
����1����� ȩ��Ƿ��������ȩΪ�Ʊ�����ø�꿹����õ�ż�������������ȩ������������ᡢ��ϩ�ͼ����ȩ�����ۺϱ������ʣ����贿����ʹ�á����ȩ�Ĵ����ú����ʵĶ�ȩ�ĵ������ȩ��OD��ֵ��ʾ�����ǵ�������չⲨ���ֱ�Ϊ235nm ��280nm�����ߵ�OD��ֵ��235/280��С��3ʱ���Ʊ�ø�꿹���Ч���Ϻã�����3ʱ���辭�����Sephadex G-10�����������̼�����ȴ�������ȥ���ʺ�Ӧ�á����Ʊ�������һ������������������ԭ����ͬ����ʹ���ȩ������ȩ��֮һ��ø�����������ϣ���һȩ�����������ϵİ�����ϣ���ø�����ڿ����ϡ�
������1��һ��������ø�����塢���ȩ��һ��������ϣ�������ȥ�������ʣ������ȩ���Ƶ�ø�꿹�塣�ŵ��Ǽ�ʡʱ��ȱ���Ƿ�Ӧ�̶Ȳ��ױ����ƣ���Ϊø�����ӺͿ��嵰����ͬ���ȩ��ķ�Ӧ���ʲ�ͬ�����嵰�İ�����Զ��HRPΪ�࣬�����ȩ��Ӧ�죬��������ȩ�������£����嵰����ͨ�������ںͷ��Ӽ�ı˴˽������γɽϴ�ľۺ��壬����ø�����Ӽ�Ľ�����Ӧ���٣�Ӱ��ø�ı�ǡ���Nakane�����㣬�����HRP��20%�뿹�����ᣬ����ʽϵͣ�Լ1%��5%�����ѻ�������ø�꿹�塣
������2���������������ù��������ȩ��HRP��Ӧ��HRP�����ȩΪ1��105�����Ա�֤ø���ӽ������ȩ��һ��ȩ����ϣ���һ��ȩ�����룻Ȼ���ò�������ȥ��������ȩ���Ƴɻ���HRP��HRP-���ȩ��������ټ�������Ŀ��壬ʹ�HRP��ʣ���ȩ���뿹�嵰�����ϵİ�����ϣ��Ƴ�ø�꿹�塣�����Ŀ�����Ա�֤ø�뿹���������ᣬ����ø�����ۺϡ��������õ�HRP�뿹�壨IgG��������ͬ��ø����ʸ��죬ƽ��Ϊ5%��25%����Dz������£�
������10��15mg HRP(RZ=3.0),�ܽ���0.2ml 1.25%���ȩ�У�0.1mol/L���Ỻ��Һ���ƣ���18h���¡�
���������� Sephadex G-25��������0.15mol/l NaClƽ�⣩��ȥ�����������ȩ���ռ��HRP��
������Ũ���HRP��10mg/ml���ң����뿹��5mg(1.0ml 0.15mol/L NaCl �ܽ�)��
������̼���λ���Һ��pH9.5������pH��9.0��9.5,ʹ������HRP��ϣ�4��24h��
�����ݼ���0.1ml�����Ỻ��Һ�����δ��Ӧ��ȩ����4�棬2h��
�������ð뱥������麟���5�Σ���PBS��24h��4�棬��3��PBS����ȥ����泥�10000rpm/min,30min����
������������ɫ����Sephadex G-200/Sephacryl S-200�� �ȷ����ǿ��塣
����ע�⣺�÷���Ҫ��HRP��RZֵ��3.0���ң����백�����٣������ȩ��Ӧ���Ƴɵ�ø�꿹���Ϊ���壻��RZֵС��2.8��HRP�����н϶�����백���������ȩ��Ӧ�����γɶ���壬ʹ�������������½���
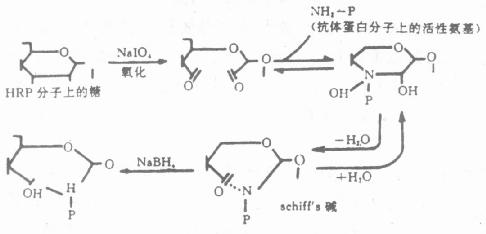
����2���������������������ϸ�ؽ����������ƣ�Sudium periodate������һ��������ż�������䱾��������Ϊ�������ڿ����ø֮�䣬���ǽ����ڹ������Ƶ��������ã���ø�����ڿ����ϡ��÷��������ں��ǽϷḻ��ø����HRP���ı�ǡ�����֪����HRP���ӵ��DZ�����ø�����أ����ù������������ⲿ���Ƿ����ڵ�-CH����ʹ֮����-CHO�������뿹�嵰�����백����Ӧ������Shiff��s���Shiff������pH����ʱ�ʿ����Խ��룬���Ծ������ƣ�NaBH4����ԭ���γ��ȶ���ø�꿹�帴���ͼ4-1����Ϊ��ֹ���ɵ�-CHO����ø���װ�������������Ԥ�ȿ��ö�����������Dintro-fluorobenzene������HRP����Ϸ����ڵĦ�-����-������

ͼ4-1��������������ԭ��
��������������������ø��RZֵ��3ʱ�ϼѣ�RZ<3ʱ���Ǻ������٣����백���϶࣬����ʱø���������ۺϣ�Ӱ��ø�꿹��IJ������ݱ��棬�ʵ��ؿ��ƹ���������Һ����Ӧ�����������������HRP�Ϳ�����γ�ø�꿹�壬������Ϊ70%���ҡ����岽��Ϊ��
������1��4mg HRP(RZ=3.0)����1.0ml˫��ˮ�С�
������2����0.2ml�������Ƶ�0.1mol/LNaIO4������ҡ�����20min,���ۿɼ�Һ�����ػƱ������ɫ��
������3����0.1mol/L�����λ���Һ��pH4.4������20h��4�档
������4������HRPҺ���pH��9.5(һ�����20��l0.2mol/L̼���λ���ҺpH9.5),�������뿹��(IgG)8.0mg/Fab 3.0mg (0.01mol/L̼���λ���Һ�ܽ�),������Ⱥ�,������2h��PH��8.5ʱ,�����NH2������������NH3+,���߲�����CHO����Ӧ,����,����pH9.0��9.5�dz���Ҫ��
������5������0.1ml�������Ƶ�0.4%NaBH4 ��Һ����1��4��2h�����ȶ�ø�꿹�帴���
������6��������ȥ��δ��Ӧ��NaBH4 �����ԭ���ȡ�Ȼ���������������ȷ�������ø�꿹�壨����ͬ���ȩ������
��������Ƶõ�ø�꿹�壬������Ũ��1%ţѪ����ף�Bovine Serum Albumin, BSA����װ����-80��ɱ������ꣻ��ɼ���6%�������ͣ�������-20��/4�汣��1�����ҡ��������ֱ�Ƿ���ICC�о�����õ�ø�꿹���Ʊ�������
����3��Maleinmide������ ����ø�꿹�壨IgG���ķ������ϴԿ���Ĵ�����һ��Ӱ�죬�����Ʊ������У��辭���δ�������������뵥�弰������DZ�ǿ���ķ��롣��֪���壨1��HRP���ӱ��1��IgG���ӣ��ķ�����Ϊ190��200kD���DZ�ǿ���Ϊ146��150kD�����������˷����ѽ����߷ֿ�������,Sternberger�Ƚ����˿���Ƭ��Fab�ı�ǡ���ֲ���Ե���ø---ľ��ø��Papain��ˮ�⿹�嵰�ף��ɻ��һ����������ȶ���Fc�νᾧ��������ͬ�Ŀ�ԭ���Ƭ�Σ�Fab������Fab��Ϊ���ۣ�������50kD,HRP��Ǻ��������Ϊ90kD,����������ͷDZ�ǵ�Fab�η��롣�ڴ˻����ϣ�Imagawa(1982)�ֽ����˸�����������N-�ǻ�����������Maleinmide������ǿ�����ض���λ---Maleinmide�����÷�������Ҫԭ���ǣ���1������˫�����Լ�Maleinmide�HRP��ʹ������롪Hs ����Ӧ����������2������θ����øˮ��IgG��IgG�����ڽ��Ȼ��˱��жϣ������ڽ�������Hinge region�����ٿ��Ա���һ��S-S�����Ӷ��õ�һ������˫�ۿ�����Ե�F��ab����2�Ρ���S-S���뿹������ء�����ͨ����������Ҵ���2���£�-Mercapto ethanol, HSCH2CH2OH��ʹ����ѣ�����ԭ�ɡ�HS�� �����˫�ۿ�����Ե�F��ab����2Ƭ�μ���Ϊ���С�Hs ���ĵ���Fab��Ƭ�Σ�����������HRP��ϣ����Ƴ���ø�꿹��Fab�������ڿռ��ڱεĹ�ϵ����������ʹ����������HS����Ҳֻ����һ������ø��ϣ���һ����HS��������ø��Ӧ����ø�뿹��Fab���ν�ϱ���Ϊ1��1�����ø�꿹��Fab���ξ�������ǵ��壬�����γɶ���塣�ڱ�ǹ����У�Ӧ�ù����ĻHRP�����ܱ���DZ�ǿ���Fab���εĴ��ڡ�Fab���εķ�������Fab�����ƣ�50kD���ң�������ø���Fab�����������δ��ǵ�Fab�����롣�˱�Ƿ���������ø���߷����о����䲽��Ϊ��
������6mg HRP����1.0ml PBS(pH7.0)��
������4mg Maleinmide ����0.5ml N, N����������N,N-dimethylformamide����
�����۽���������Һ���ֻ�ϣ���������1h,30�档
����������ȡ���壬��0.1mol/l PB(pH6.0)ƽ���Sephadex G-25���������ռ����е��ײ��ֵ�ϴ��Һ��Ũ�����ƵûHRP��
������ÿ1.8mg�HRP�������ѱ���ԭ��Fab��2mg,4��20h�������衣
������ Sephadex G-200/Sephacryl S-200����ø�꿹��Fab��Ƭ�Σ�����ͬǰ��
����������ø�꿹��Ĵ���
�����������ַ����Ʊ�ø�꿹��ʱ��������ø�꿹���⣬����δ��ǵĿ��嵰�ס�����ø��ø�����弰ż�����ȡ���Щ����ʹø�꿹����������½�����ø�꿹���뾭������Ӧ�á��ּ�鼸�ֳ��õĴ���������
����1�������ķ��롡��ʵ���У���ͬ���Լ��γɵĶ������������죬��ʹͬ����ʵ��ҩ��ͳ����ڲ�ͬ��ʱ���Ʊ���ø�꿹���У��������������ͬ�������ϵ��庬ø���࣬����֯�ķ�����������ǿ��ʹ�������������½�������ǰ�����ȥ����塣���������˷����������Ч���Ϻá�
����2���DZ�ǿ���ķ��� �����DZ�ǿ������ǿ��������ͬ������ѧ�������ܾ�������֯���쿹ԭ��ϣ����������ϱ�ǿ���ǿ����������֯��ԭ��ϡ�һ����Ϊÿ����������1��2��ø���ӣ�����Ӱ�쿹���������Fab����ԭ��ϵ㣬������ڿռ��ڱ�����һ��Fab������֯�����Կ�ԭ��ϡ��DZ�ǿ�������������������Fab�ξ��뿹ԭ��ϣ����������ǿ������ø�꿹����Ӧ��ǰ������֬���ϲ����ȷ���ȥ���DZ�ǿ��塣
����3���ϲ��� �����õ���A��Protein A��/��֬��-������A/��֬���ϲ��������Ƶýϴ���ø�꿹�塣��Ϊ����A�뿹�壨��Ǻ�δ��ǣ����н�ǿ������������HRP��ϡ���������A��HRP����Ǻ����룩��������dz�ǿ�����뿹���ϡ��ݴ˶��߲��ã��ܻ�ýϴ���HRPø�꿹�塣�÷���ʡʱ����������ǿ��ԼΪ����������600����������һ���ľ����ԣ���Ϊ����A������������������������������ǿ���������������������ϣ������������ڴ������ø�꿹�塣��������A��HRP��������ǿ�������ʲ������Խ�ϣ���ʹ����ø�꿹��Ļ���ɥʧ��
�������ģ�Ⱦɫԭ��������
����1������ԭ������ø�꿹����ӫ��ɫ�ر�ǿ����Ⱦɫ��ͬ�����ֱ�ӷ��ͼ�ӷ���ֱ�ӷ��ǽ�øֱ�ӱ����ÿһ�����ϣ���ӷ��ǽ�ø����ڵڶ������ϣ������֯ϸ���ڵ��ض���ԭ���ʡ���ӷ����õĵ�һ�����Ƕ���֯ϸ����ij�ֿ�ԭ�������Կ��壨80%��90%�Ŀ�Ѫ��ϵ�ɼ����Ƶã�������������¡����ϵ��С���Ʊ������ڶ�������Ϊ��һ���壨����/С���IgG���Ŀ��塣���ԣ�ֻҪ��ͬ�ĵ�һ���������ͬһ������ͬһ��ǵĵڶ��������������ʾ�䲻ͬ�����Կ�ԭ�Ĵ��ڣ������ɱ�����ֱ�ӷ��б��ÿһ�ֵ�һ������鷳����������˷��������жȡ�Ŀǰ��ICCȾɫ�У��Լ�ӷ�Ϊ���ã��ڴ����ؽ��ܼ�ӷ���Ⱦɫ����
����2��Ⱦɫ����
������1����Ƭ��������һ�¡���
������ʯ����Ƭ�����ױ���Hemo-De���������оƾ���ˮ���ڹ̶�/�̶�������֯������Ƭ�����¸���2h���ϡ�
������2��δ�̶���������֯��Ƭ����ͪ�̶�20��30min(fretrieval )�������֮�����õ���ø������ȥ���̶���������ɵĿռ��ڱΣ����£������15��30min.;�ѹ̶�����֯������Ƭ��ʯ����Ƭ��������Ҫ�ɽ�����֯��ԭ�ļ��
������3������������Ƭ��Χ����һ�����ϣ��Ա������Һ��ʧ��������������Ƭ���ͬʱҲ�ܽڡ�ʡ����������������Ƭ�뿹��ij�ֽӴ�����ɡ�ʯ����Ƭ��������PBS���Է�����ֱ�ӽ��в��裨6����
������4����Ƭ��PBS����������ҺƯϴ3�Σ�ÿ��2min���ܽ��ȥ������Ƭ�ϵ�OCT���������Ӧ��ALP��ǿ���ʱ�����ö��������ƻ���ҺƯϴ������߿�ʹALPʧ�
������5��������Ҫ���ü״�+0.3%H2O2������Ƭ15��30min�����£��������Դ�Թ�����ø�Ļ��ԡ�Ӧ��ALP��ǿ���ʱ���˲���ʡ�ԡ�
������6��PBSƯ ϴ2min�������Σ�������0.05%Tween-20/PBS(��0.22��1%Triton X-100)��5min�����£���Tween-20Ϊһ�ֱ�����Լ�����������������⣬����������֯��ͨ�ԣ���������֯ϸ���ڿ�ԭ����ʾ��
������7��4%Block Ace��0.1%��1%BSAʪ���ڷ���15��25min�����£���Ȼ��������ȥ����Һ������ϴ�����������֯�뿹��ķ������Խ�ϣ����ͱ���Ⱦɫ��
������8��������Ҫ������1/5��1/30����������/��Ѫ�����15��20min�����£���ø�꿹����ͬ��������Ѫ��Ϊ�ˣ������ͬһ��������ǰ��Ѫ�壩������ʡ�Դ˲�������ϡ��ø�꿹��ʱ������1%��2%��ͬһ��������Ѫ�塣
������9��������ȥ����Һ�� �μӺ�0.2%BSA/0.05 NaN3/PBSϡ�͵ĵ�һ���壨����������ÿ����Ƭһ��Ϊ50��80��l����ʪ���ڷ���1��2h��20��25�棩�����ߵ羵�ñ걾��4���ҹ��
������10��PBS��ֳ�ϴ��3�Ρ�2min������ȥ����Ƭ�Ϸ����������Ŀ��塣Ӧ�ò�ͬ�ĵ�һ�����ͬʱ���ж��ձ걾Ⱦɫʱ����ֱ��ϴ���Է����Ⱦ��
������11����0.05%Tween-20/PBs 2min��,�μӺ�0.2%BSA/1%����Ѫ��/PBSϡ�͵�HRPø��ǵĵڶ�����,ʪ���ڷ���45��60min(20��25��)��
������12��PBSƯϴ��3�Ρ�2min��,�˴�����ֱ�Ưϴ����������Ƭ��ϵͬһø�꿹�������
������13��δ�̶���̶������ı�����Ƭ���˴������̶������Ƚ���Ƭ��PBS����TBS��3��5min��ȥ��PBS���Է����е����������ʹ�õĹ̶�Һ�е�CaCl2�γ�����ƶ�������Ȼ����Baker�Ϲ̶�Һ�̶�5min�����£���ʱ���̶����Ȳ�Ӱ�쿹ԭ�����ϣ��ֽ������ڱ����һ�������ǰ����֯��ԭ�����������ڵ���¡�����ICCȾɫ��
������14����ɫ��HRP��ǿ���ij�ɫҺΪ0.01%��0.1%H2O2 0.01%��0.05% DAB 0.05��0.1mol/L Tris �CHCl(pH7.4)����Ƭ��PBS��Tris-HClҺƯϴ����������ɫҺ��10��15min�����¡�����������ɾ��¿�����ɫ�ٶȡ��ղ���Ϊ�غ�ɫ���������ڵ羵�۲�ı걾����ɫ3��5min���ɣ���ֹDAB�ղ�������Χ��ɢ��Ӱ�쳬�ṹ��λ�����⣬��ɫҺӦ����ǰ�������ƣ�����DAB�����������ʡ������Ƶ�DABΪ��ɫ��Һ�塣��DABҺ��������Ϊ�Ϻ�ɫ��Ӧ����ҩ�������ơ�
������15������Ƭ����ˮ�У����⾵�۲죩��PBS���羵�걾���ڣ���ֹ��ɫ��Ӧ��
������16��δ�̶��ı�����Ƭ������1%���ȩ-PBSҺ��ǿ�̶�5��10min�����£�����ˮ��ϴ��
������17��ϸ�������Ⱦɫ���Լ��̺���ľ��Ϊ���á�ǰ��ϸ���˳���ɫ����HRP/ALP���ղ���Աȶ��ȼѣ���������������ı걾����ľ������֯ѧ������ѧ�о����ձ�Ӧ�õĺ�Ⱦɫ��������HRP��ALP���ղ���ԱȶȱȽϺá�
������18��DAB��ɫ�ı걾������ϵ�оƾ���ˮ��Hemo-De����DPX��̡��������ʳ�ɫ�ı걾�����л��ܼ��г��������ܽ⣬��ɫ��������ˮ���Է�̼����������͵ȷ�̣����գ��ڸDz�Ƭ��ΧͿ����Ůʿ��ָ���ͣ���ʹ��Ƭ����ʱ�������
������19�����졢�۲��¼ͬһ����̬ѧ�о���
������20�����ߵ羵�ñ걾����OSO4��̶������羵�걾Ҫ�������μ���������¡��������OSO4�̶�����̼��Carbon Coating��,����ɨ��羵�۲쿹ԭ�Ĵ��ڲ�λ��
����3��ø�꿹�弰��ɫ����ѡ��

����HRP�������ΪH2O2,�ڷֽ�H2O2������,��H2O2�γɸ�����,���ӹ������ʱ,��Ӧ���ٽ���,�����ӹ������ʱ,Ѹ������ˮ,ø����ԭ,���ӹ��屻��������,�γɱ����ݾۺ���(ͼ4-2)����ø��Ӧ��λ���γɲ������غ�ɫ����������֯�Ա�������
����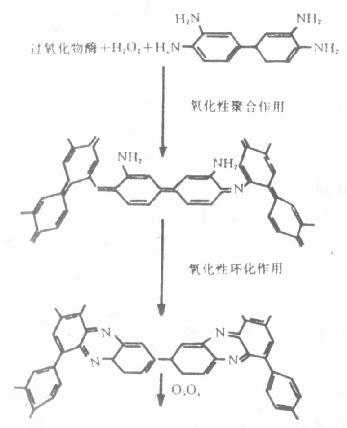
ͼ4-2 DAB��Ӧ�����γɹ���
����HRP����ø�ٷ�Ӧ��һ���������Եġ�ø������H2O2�����෴Ӧ�Ƿ�����ģ����ø��ֵ��ӹ���鵼������ѡ�ò�ͬ�ĵ��ӹ��壬��ʹ�ղ���ʲ�ͬ��ɫ�����磺CN��4��Chloro��1�C N aphthol��Ϊ����ɫ��TMB��Tetramethyl��Benzidine ��Ϊ����ɫ��AEC��3��amino��9�C ethyl--carbazole��Ϊ��ɫ�������Լ���������ɫҺ��AEC�Ӷ࣬�����½��ȶ��������ܽ�����ˮ�ȴ�������ʱ�䳤����ɫ��DAB�ǹ㷺Ӧ�õĵ��ӹ���֮һ�������У���Ƭ����ˮ���������ñ��棬���ղ�������ȶ��ԣ���O2O4�����������ܶ����ӣ����ڵ羵��ȷ����ԭ�Ĵ��ڲ�λ������DAB����Ϊ���ܾ����°��ԣ�����Ӧ������������ͽӴ���������ý�DAB�Ƴ�10������Һ����װ��-20�汣�棬Ӧ��ʱϡ�͡����ˡ���DAB�Ƚϣ�CN�������Բ�������ղ���Ͼ��ޣ�������ɢ���⾵�۲��Ϊ�ʺϡ�
������2��ALP������As-MxΪ���FB/FRΪ��ɫ�ţ�������ɫ/��ɫ�����Գ�����ALP��ǿ�����Ҫ������Դ�Թ�����ø�����ϸߵ�Ѫϸ�����ܰ�ϸ���ȵ�ICCȾɫ����ɫҺ�ڼ�����Ũ��Ϊ2��4mmol/l ��levamisole, �������Դ��ALP���Կɱ����ơ�ͨ����������levamisole����ÿ����60��120mmol/LŨ�ȵ�����Һ-20����䱣�档Ӧ��ʱϡ��30����Ϊ���ⷴ����ȡ���Լ���ˮ��As-Mx��FR��FB�Լ���ӦС����װ��-20����䱣�棬����������������Դ�Լ�������ø���ԡ����磺��ÿ��������ɫҺ30ml���㣬��װAs-Mx 5��7mg/֧��Fr 8mg./֧��FB7mg/֧��ÿ��ʹ��һ֧����ǰϡ��30����������ɫ ��FR��FB���ڹ��������������������������ɫ��Ӧ�ڰ������С�
������3��GOD������������Ϊ�����ø������ɫ����Ϊ��-D-������67mg��NBT6.7mg��PMS��Phenazine Methylsulfate��0.167mg,0.05mol/L PB(pH8.3)10.0ml,37�����1h��������ɫ�����Գ��������ղ��ﲻ�����л��ܼ�����Ƭ����ˮ�������ڱ��档��GOD�����жȽ�HRP��ALPΪ�ͣ����ӹ����٣�Ӧ�ýϾ��ޣ���Ҫ��������ø�ķŴ���������߷����������Ժ������ԡ�����GOD��HRP�ֱ��ǵڶ����������壨����һ����ΪС��¡���塢�ڶ�����ΪGOD��ǵ��ÿ���IgG������������ΪHRP��ǵ�����IgG����ICCȾɫ����������-DAB����ɫ��������ԭ���磨ͼ4-3����������HRP����Ϊ�ڶ�øϵͳ����������������ʱ���ɵ�H2O2�������ø�ٷ�Ӧ��������Դ�Թ�����ø��Ӱ�졣����GOD��HRP����ǵĿ����ǽ����ͬһ��ԭλ�ã����������õ���ʾ��֯��ԭ�Ĵ��ڡ�����ҪȾɫ����Ϊ��
��������Ƭ����һ���ķ�������Ưϴ��GOD��ǵĵڶ��������40��60min�����£�����Ưϴ��HRP��ǵĵ����������30��45min�����£�����Ưϴ����ɫ����ˮ���۲�ͬǰ��
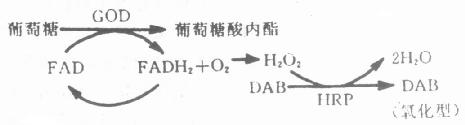
ͼ4-3������ø����Ӧԭ��
���������DZ�ǿ���ø��
��������ø�꿹�����һЩȱ�㣬�����ø�뿹���Ĺ�����������ֿ����ø�Ļ��ԣ��ڿ�Ѫ���еķ������Կ��屻ø��Ǻ�����֯�ɷֽ�ϣ����±���Ⱦɫ�ȡ�Ϊ��Sternberger����ø�귨�Ļ����ϣ���չ�˷DZ�ǿ���ø��������ø�ŷ���Enzyme Bridge Method����������ø����������ø����Peroxidase Antiperoxidase Method, PAP�������ַ������¡�
������һ��ø�ŷ�
����1������ԭ������������ø���߶���Ʊ�Ч�۸ߡ�������ǿ�Ŀ�ø���壬Ȼ��ʹ�õڶ��������ţ�����ø��������������֯��ԭ��ϵĵ�һ�����ϣ��ٽ�ø����ڿ�ø���壬����ɫ��ʾ��ԭ�ķֲ����ڴ˹����У��κο����δ��ø��ǣ�ø��ͨ������ѧԭ���뿹ø�����ϣ������˹�������Կ����ø���Ե�����߷����������ԣ����ܽڡ�ʡ��һ�����������
����2��Ⱦɫ���� ��Ҫ������ͼ4-4
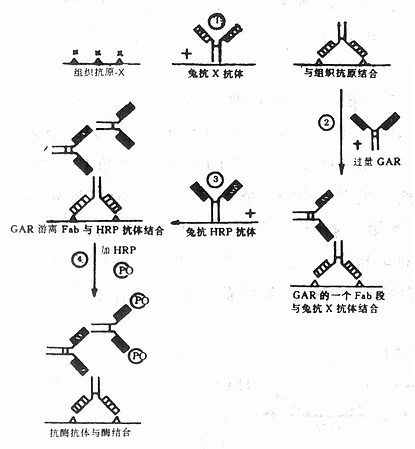
ͼ4-4��ø�ŷ���ҪȾɫ����
������1����Ƭ������һ�������ǰ����ͬ��ӷ�����һ���壨������������A������24h��4�棩����һ�����ϡ�Ͷȿɸ�Щ��ʹ���������Fab�ξ�����֯��ԭ��ϣ����ι̣�Ưϴʱ����ʧ��
������2����Ƭ��ڶ����壨Ҳ���ſ��壬������a IgG���壩����1��1.5h�����£���Ӧ�ù������ſ����ܱ�֤һ��Fab�����һ�����ϣ���һ��Fab�����롣
������3����Ƭ�뿹ø���壨��������A������1��1.5h�����£�����ø����͵�һ�����ϵ����a IgG��������ͬ�Ŀ�ԭ�� ������ �ſ��������Fab���뿹ø�����ϣ����ŵ����ã�����ø��������������֯��ԭ��ϵĵ�һ�����ϡ�
������4����Ƭ��ø��HRp 70��100��g/ml,PBS�ܽ⣩����0.5h�����£���ø�뿹ø�����ϡ�
������5����ɫ����ø�꿹�巨��ͬ��
����ø�ŷ��˷���ø�꿹�巨��ȱ�㣬�Ϻõر����˿����ø���ԡ��������䲻�㣺����ø����Ѫ���У����е���������������壬������Ϊ��ԭ���ſ����ϣ���Ҫ�������ſ�������������������䱾����ø�������أ��ʶ��߾��ɱ��������ſ����ϡ��������Ŀ�ø������ø��Ͻ�����Ưϴʱ���룬ʹ��ø��70%���ң���ʧ�������˷����������ԡ��ڵ��������õĿ�ø����Ѫ���У��ຬ�з������Կ��壬�俹ԭ���뿹ø������ͬ�����������ſ����ϣ���������ø��ϣ�Ӱ����֯��ԭ����ʾ��Ϊ��70�������Sternberger(1970)�ֽ�����PAP���������Ը�������ΪICC�о��г��õķ���֮һ��
����������PAP��
����1��PAP���Ʊ������� ��PAP�������������Ʊ���HRP��HRP����������Ʊ������϶࣬�ּ������֮һ��
������1���Ʊ���HRPѪ�壺�������Լ��ã�2.0kg���ϣ�������������Ƥ��ע�����Ŀ����磨��10mg����2�ܺ��ظ�1�Σ��̼���������ϵͳ���ܣ�1�ܺ��ڱ�����������Ƥ�ڶ��ע��1.0ml���[��������ȫ��������HRP3.3mg(RZ=3.0)];���2�ܵ�2��ע�䣬����ע�뺬HRP3.3mg�IJ���ȫ��������1.0mg���ټ��2�ܣ���3��ע�䣬2mgHRP������2ml������ˮ�У����ֱ���ǰ��С��Ƥ�ºͱ��������ڶ��ע�䣬1�ܺ�ɾ���Ѫ�����Ч�ۡ��ٸ�1�ܵ�4�μ�ǿע�䣨����ͬ��3�Σ���һ�ܺ��鿹��Ч�ۣ���֬����ɢ����HRP0.1mg/ml��Ϊ1��128����ʱ��������ȡѪ���Ʊ�Ѫ����±��汸�á�
������2���Ʊ�PAP��������������£�ʹ�ÿ�HRP������HRP�γɿ����Ը�������Ʊ���HRPѪ��ʱ��HRP�Ĵ���Ҫ�ߣ�RZ��3�������Ʊ�PAP������ʱ��HRP������Ҫ�ߣ���������ø�Ĵ���Ʒ��
���������衿
������ȡ10.50ml��HRPѪ�壬��7.60ml��7.6mgHRP��1.0mg/ml����ˮ��Һ��
�����ڻ��ȣ�����1h������16000g 4��15min��
������0.9% NaCl(����ˮ)�ܽ����������16000g 4��15min���ظ�4�Ρ�
�����ܼ�15.3ml HRPˮ��Һ����HRP30.64mg�������£��������衣
��������1N HCl��0.1N HCl��pH��2.3��������ȫ���ܽ���壬������1N ��0.1n NaOH��pH��7.2��
�����������ӵ�����ı�������泥���0��45min��
����������35000g 0��15min��������50%�����Ưϴ���Ρ�
��������10.50mlˮ�ܽ����������Һ��48.6g NaCl, 1.5N NaOOCCH3 30ml, 3N(NH4)2SO430ml, ˮ5.94L������4�����ģ��ռ����壬����Һʹ�����10.50ml����װ���±��档
����������������
�����Ʊ���PAP������Ӧ���ø�Ϳ���ĺ������Լ���PAP����������������÷ֹ��ȼƼ��PAP�ĸ�������280nm��IgG��������ղ�������400nm��HRP��������ղ������Ĺ��ܶ�ֵ��ODֵ��������ʽ����IgG��HRP�ĺ����� ��
��
����һ��HRP/��HRP�Ŀ˷��ӱȴ�1.9ʱ���ɷ�װ�����-85����䣬�ݱ��������ص�PAP������ɱ���14��֮�ã������ı䡣��ϡ�ͺ��PAP�����ﲻ�ȶ���4��ɱ���2��3�ܡ��������ǰ���ơ�
������PAP�������������
����PAP��������γɲ�ͬ��������ԭ���巴Ӧ���ڿ�ԭ�Թ���ʱ�����еĿ�HRP����������γɿ�����PAP��������������������HRP�����������ԭ���巴Ӧ��Ҫ��ԭ���Թ��������γɿ����Ը����PAP���������״�൱�ȶ������ܿ�ԭ����Ӱ�죬�����������Ŀ�ԭ���������������γɵ�PAP��������HRP/��HRP֮�Ⱦ���Ϊ3��2��Ӧ�����ij�����Һ����ɢ�ȷ�������������PAP���������ϵ��Ϊ11.5s,������Ϊ400��430kD���ɴ˿������ø�뿹��֮��Ϊ3��2����ÿ��PAP��������3��HRP���Ӻ�2����HRP������ɣ�������νṹ��3����ΪHRP����������Ϊ��HRP���塣����H2O2-DABȾɫ���羵���Ѿ��۲쵽PAP����������λ�״�ṹ��ֱ��ƽ��21nm �����ֽṹ�쳣�ȶ����ݱ���PAP������Ŀ�HRP������HRP��ϳ���Ϊ108���ڴ˿����Ը������У���ʹ������������HRP���Ӱ�����ȶ��ԡ�
����2��PAPȾɫԭ��������
������1��ԭ������ø�ŷ����ƣ����ǽ����ſ��彫ø����������֯��ԭ��ϵĵ�һ�����ϣ�����ͬ����PAP����ø�ŷ��IJ���3��4�ϲ�Ϊ1����PAP��������棬����������PAP�����������Ƭ���ʳ�PAP����PAP�������еĿ�HRP����͵�һ����Ϊ��ͬ���������IgG�������ſ����ܹ���Ϊ���š���PAP�����������ڵ�һ�����ϡ�
������2��Ⱦɫ���裺��Ҫ������ø�ŷ����ƣ���ͼ4-5��
��������Ƭ������һ�������ǰ����ͬ��ӷ�����Ƭ�������Ե�һ�������ͬø�ŷ���
�������ù������ſ������������ͬø�ŷ���
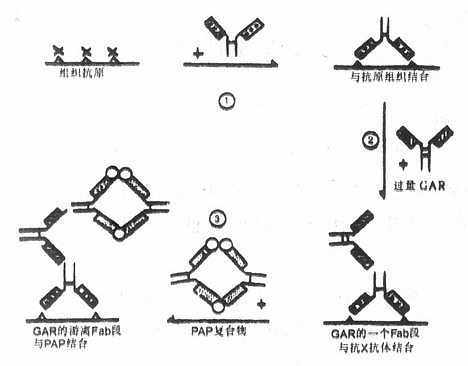
ͼ4-5��PAP����ҪȾɫ����
�������������Ƶõ�PAP�����1��30��300ϡ�ͣ�����1��1.5h�����£���ʹ�䱻�ſ��������ڵ�һ�����ϡ������ALP��ALP��������档
��������ɫ�۲��ͬ��ӷ���
����3��PAP�������ۡ���PAP��Ӧ�ñȽϹ㷺���ر��ǽ����꣬PAP��ABC���Լ�����Ʒ�����ڿ��к��ٴ�������ϵ������Ź�����ǰ��������Ҫ������ע���������£�
������1��������Ըߣ��DZ�ǿ���ø������ȵر����˿�����ԣ���Ϊ�����еķ�Ӧ�����У��κο����δ��ø���ᣬ�����˱�ǹ��̣����ۼ����ᣩ�Կ�����Ե���
������2�������ȸߣ���������ָICC�������ܷ�������������ԭ���ԡ��������Ͻ���PAP��Ӧ�ýϼ�ӷ�����2�����ϣ���Ϊø�꿹�巨�У�ø�뿹��Ϊ1��1��ǣ���PAP�����ﺬ��3��HRP���ӡ�����һ����һ����ͬһ��ø�꿹��/PAP�������ϣ��������ڿ�ԭ��λ��ø����������ͬ������PAP��Ӧ�����С�����֪����֯��Ƭ��ԭ�ĺ�����δ֪�ģ����Բ���ֱ������Ƭ�ϼ�ⷽ�������жȣ������Լ���������Ƭ��ԭŨ����Ժ㶨������������ƬȾɫ���Բ���������Ⱦɫ���õĵ�һ�������Ũ����Ϊ���������жȣ�������ȣ�Signal/moise,S/N����ʾ���ݴˣ�Sternberger(1979)��ΪPAP���ϼ�ӷ�����20��25�����ɽ�һ��ϡ�͵�һ���壬�Խڡ�ʡ����������ʵ����PAP�����ӷ�֮��IJ��첢��������ԡ�������ʵ����ע���PAP��ʾ���ԵĿ�ԭ����ͬ��ϡ�ͱ����ĵ�һ�����ڼ�ӷ���������Է�Ӧ����ʱ������ʱ��PAP����Ϊ���ԡ���ԭ���в�������������ſ���͵�һ������ʱ����ʣ�ࡱ�����룩��Fab���٣�PAP�����ﱻ�������Ӧ�����йء����� ��PAP������������ϴ�400KD��,������Ƭʱ������֯����Զ����ø�꿹�壨������90��180kDa�������Բ��������ߵ羵�ı걾������
������3������Ⱦɫ�ͣ���ø�꿹�巨�У�����ǵķ������Կ��������֯�ɷֽ�ϣ���ɱ���Ⱦɫ��ͼ4-6�����������Ͻ����ڷDZ�ǿ��巨�����Ό���У���ʹ���ŷ������Կ��壬���䲻�ǿ���һ��������IgG�������Կ��壬������뿹HRP�����ϣ����ܰ�PAP�����������ڴ˷������Կ����ϣ�ͼ4-7������Ȼ��PAP��������Ҳ���ܴ���Щ�ǿ�HRP�Ŀ��壬�����ⲿ�ֿ����ܹ����ſ��弰��֯�ɷֽ�ϣ������䲻�ǿ�HRP�Ŀ��壬�ʲ�����HRP��ϣ���ø���ԡ����˵�ſ�������룬ʹICC�������Եõ���˫�طŴ�S/N����Ҳ������Ϊ���������ſ��弰PAP������Ⱦ�����Fc�����ϣ���ʹ����Ⱦɫ��ǿ��ʵ����������ʵ���Ƭ����ǡ����Ӧ�÷������ϼ�������Ѫ������Ϸ������Խ�ϣ���֮�ʵ���ѡ����ϡ�ͶȺ�������Դ��ø���ԣ�PAP���ͼ�ӷ����ߵı������൱�͡�
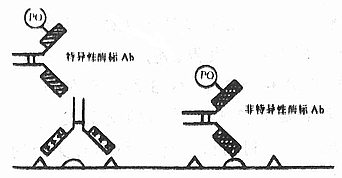
ͼ4-6�����ø�꿹�巨
������Ⱦɫ����ԭ��
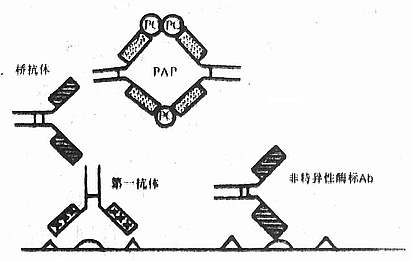
ͼ4-7��PAP�����ͱ�����ԭ��
������4�������Լ��䴦����Ӧ��PAP����ʾ��ԭ�����϶����֯�������Ƭ��֯��ԭ�������õı걾ʱ���ɵ������Խ�������������Ϊ�����ԡ�Vandesand���֣�Ӧ��PAP����ʾ�������Ϻ˺����Ժ��ڼ�ѹ����ϸ���ֲ�ʱ����һ���壨1��200��Ⱦɫ����ѹ�غ���ϸ����ǿ�ԡ����ȡ��ǰ24��48h��������ע����ˮ���أ������ͻ�������������Ϻ˺����Ժ˼�ѹ�غ�����ͬʱ��֯�걾����ˮ��������ˮ���ȴ��������ӿ����ͨ�ԣ�ͬ��ϡ�Ͷ�Ⱦɫ�����ȴ���ԡ���һ��ʵ�鷢�֣����ӿ����ϡ�Ͷȣ���ʼ��������Ⱦɫ��ϡ����1��1500ʱ��Ⱦɫ��ǿ���������ӿ���ϡ�Ͷȣ�Ⱦɫǿ�����½���Bigbee��1977����Ϊ�������ǵ�һ����������������֯��ԭ��Ϲ��࣬ʹ�������������Fc�μ�ľ��루d��ǡ�������Ό�������Fab����֮��ϵij��ȣ��������Ό�岻��������Fab�Σ���ʣ���Ե�Fc�Σ����Բ��ܽ�PAP����������������֯��ԭ��ϵĵ�һ�����ϣ�������ԣ�ͼ4-8������ˣ�����PAP���о���֯��ԭ�ֲ����ر���������֯������Ƭ��֯��ԭ����Ϻ�ʱ����һ���御���ø�ϡ�Ͷȣ���������ԡ�ʯ����Ƭ���ٷ���������������PAP����ʯ����Ƭ��ICC�۲��и�Ϊ���á�
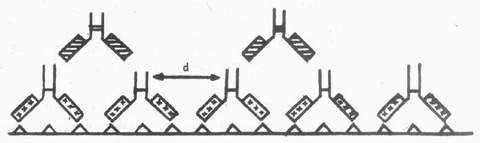
ͼ4-8��ʾ�����ԣ���֯��Ƭ�Ͻ�Ϲ���ĵ�һ���壬�������ľ���d ǡ�������ſ��������Fab����֮��ϣ���PAP�������ϵ�λ��
������5���ſ��壺Ҳ�����Ό�壬��������Fab�ξ�����ͬ�Ľṹ�����ʼ��뿹ԭ��ϵ���������ˣ�����һ�����PAP�������п�HRP��������ͬһ��������ʱ���ſ�����ͬʱ���������ֿ����ϣ����ŵ����á�Ϊ��ȷ���ſ��������Fab��֮һ���һ�����ϡ���һ���뿹HRP�����ϣ��ſ������ø�Ũ�ȡ����⣬�ڷDZ�ǿ���ø���п��������������A��SPA�������ſ��壬����ICCȾɫ��SPA�����������ƣ�Ӧ�÷�Χ�㡣
������6��PAP�������PAP����ø�ŷ��У��ر�ǿ����һ����Ϳ�HRP�����������ͬһ�������ſ�����ܷ����ŵ����ã�����������һ�𣻵�һЩ�о���������һ����Ϳ�HRP�������Բ�ͬ���������Ό���Կ���Ϊ�ţ�����������һ������Erlandsen��������IgG��Ϊ��һ���壬��������IgG����PAP��������ʾ֮һ��Grzanna��1982��������һ���棬��������DBHѪ������һ���壬����IgGΪ�ſ��壬12����Ѫ���Ƶõ�PAP�������У���3��Ⱦɫ�ϼѡ����ֵ�һ�����PAP���������Բ�ͬ������õ����Խ����Ҫ������������Ľ��淴Ӧ������ʵ�������������������淴Ӧ�����ģ�Ҳ�Dz���ȫ�ġ��������ſ������ICCȾɫʱ�����Ե�һ����Ϳ�ø��������ͬһ����Ϊ�ˡ�